Système NanoStar® NGS HLA – Dispositif médical de diagnostic in vitro – classe C, réservé aux professionnels de santé
Greffe de Moelle osseuse
Transplantation d’Organes
Inscription Registre Donneurs Volontaires
Le système NanoStar® NGS HLA est destiné au typage HLA en haute résolution dans le cadre des indications suivantes :
- Typage HLA dans le cadre d’une greffe de moelle osseuse,
- Typage HLA dans le cadre de la transplantation d’organes,
- Typage HLA des donneurs volontaires de moelle osseuse.
Ce dispositif de diagnostic in vitro est destiné à être utilisé uniquement par du personnel de santé dûment qualifié, dans des laboratoires accrédités pratiquant le typage HLA.
Kits NanoStar®
Les kits de typage NanoStar® NGS HLA ciblent les 11 loci principaux, avec une couverture complète des exons et des zones d’épissage.
Ils sont conçus pour générer des résultats de typage HLA en haute résolution, en moins de 48 heures.
Les kits sont validés pour une utilisation avec le séquenceur MiSeq® (Illumina).
Composants des kits :
- Bio-Nano® Primers
- Bio-Nano® Index Mix
- Bio-Nano® Buffer
- Bio-Nano® Seq Primers

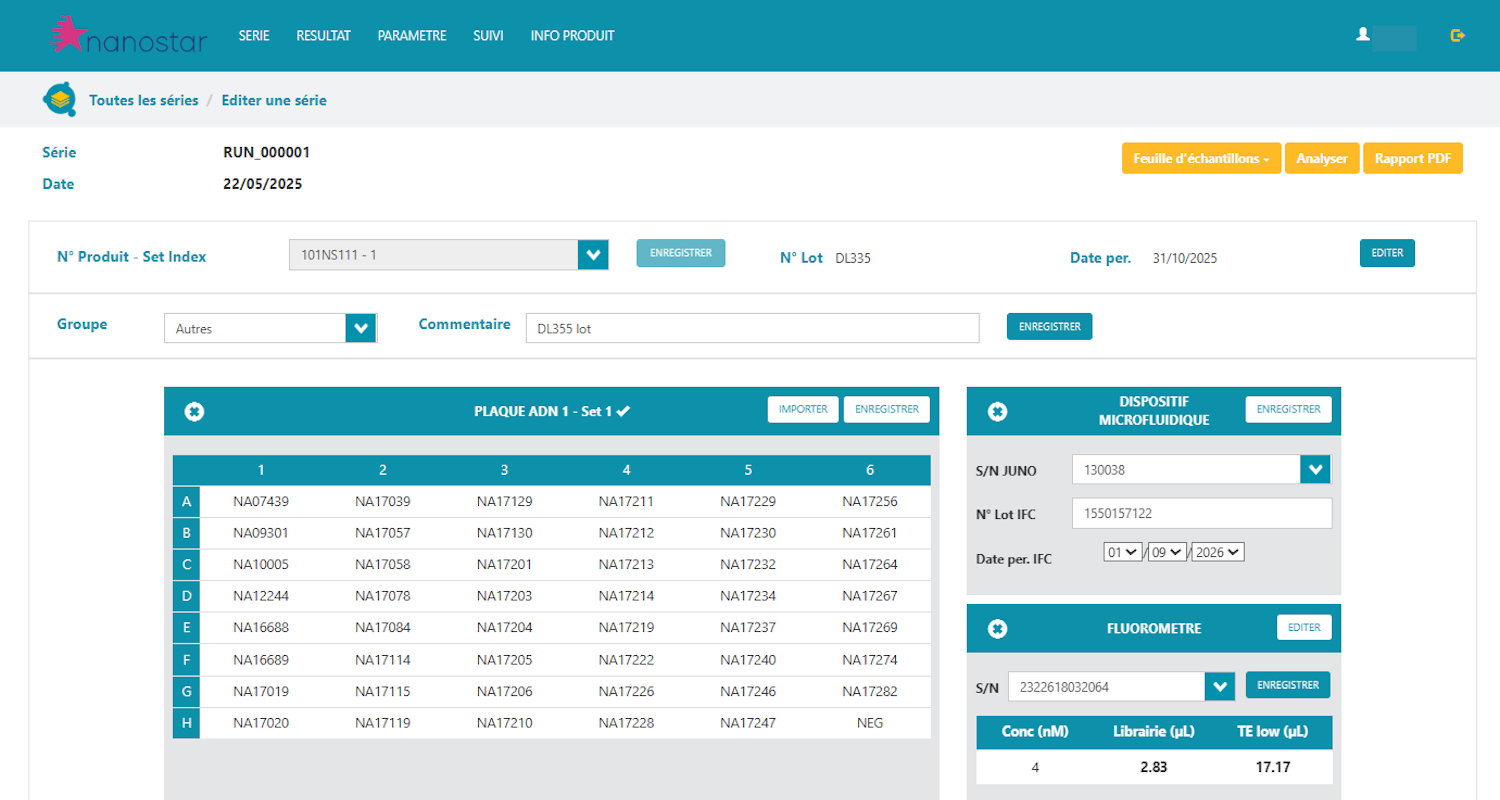
Descriptif de la méthode
NanoStar® NGS HLA repose sur une méthode de PCR indexée Short Range, couplée à une préparation de librairie automatisée utilisant la nanotechnologie et la microfluidique
L’ensemble du processus est conçu pour :
- Standardiser les étapes de préparation,
- Réduire le temps de manipulation en laboratoire,
- Assurer une meilleure reproductibilité des résultats.
Invitation à lire la notice
Nous rappelons aux professionnels de santé qu’il est indispensable de lire attentivement les notices d’utilisation NanoStar® NGS HLA (kit et logiciel) ainsi que l’étiquetage du dispositif avant toute utilisation. Ces documents fournissent les informations nécessaires à une utilisation correcte, sûre et conforme aux performances attendues.
Limites d’utilisation
Les kits NanoStar® NGS HLA sont des tests qualitatifs destinés à une aide au diagnostic dans un contexte de greffe. Les résultats obtenus ne doivent pas être utilisés comme unique source d’information pour la décision clinique. Le produit est destiné exclusivement à une utilisation en laboratoire par du personnel dûment qualifié et formé aux techniques de biologie moléculaire.
Conformité réglementaire
Dispositif médical de diagnostic in vitro (Règlement UE 2017/746 – classe C), le dossier initial de marquage CE est en cours d’évaluation,
Produit non destiné à un usage direct par le patient ou le grand public,
Notices d’utilisation et fiche de données de sécurité disponibles sur demande ou sur notre site,
Certificat ISO 13485 : 2016.
Cette communication n’est pas soumise à une autorisation préalable de publicité.
Vous pourrez télécharger les notices d’utilisation des kits et du logiciel NanoStar® NGS HLA depuis la section de téléchargement du site en nous adressant une demande pour recevoir votre identifiant.
Informations réglementaires et responsabilités
- Bionobis est certifié ISO 13485 : 2016,
- Le système NanoStar® NGS HLA est un dispositif médical de diagnostic in vitro de classe C, selon le règlement (UE) 2017/746 (IVDR), le dossier initial de marquage CE est en cours d’évaluation,
- Tout incident grave survenu en lien avec le système NanoStar® NGS HLA doit faire l’objet d’une notification à Bionobis et à l’autorité compétente de l’État membre dans lequel l’utilisateur et/ou le patient est établi,
- Produit destiné uniquement aux professionnels de santé,
- Cette communication n’est pas soumise à une autorisation préalable de publicité.
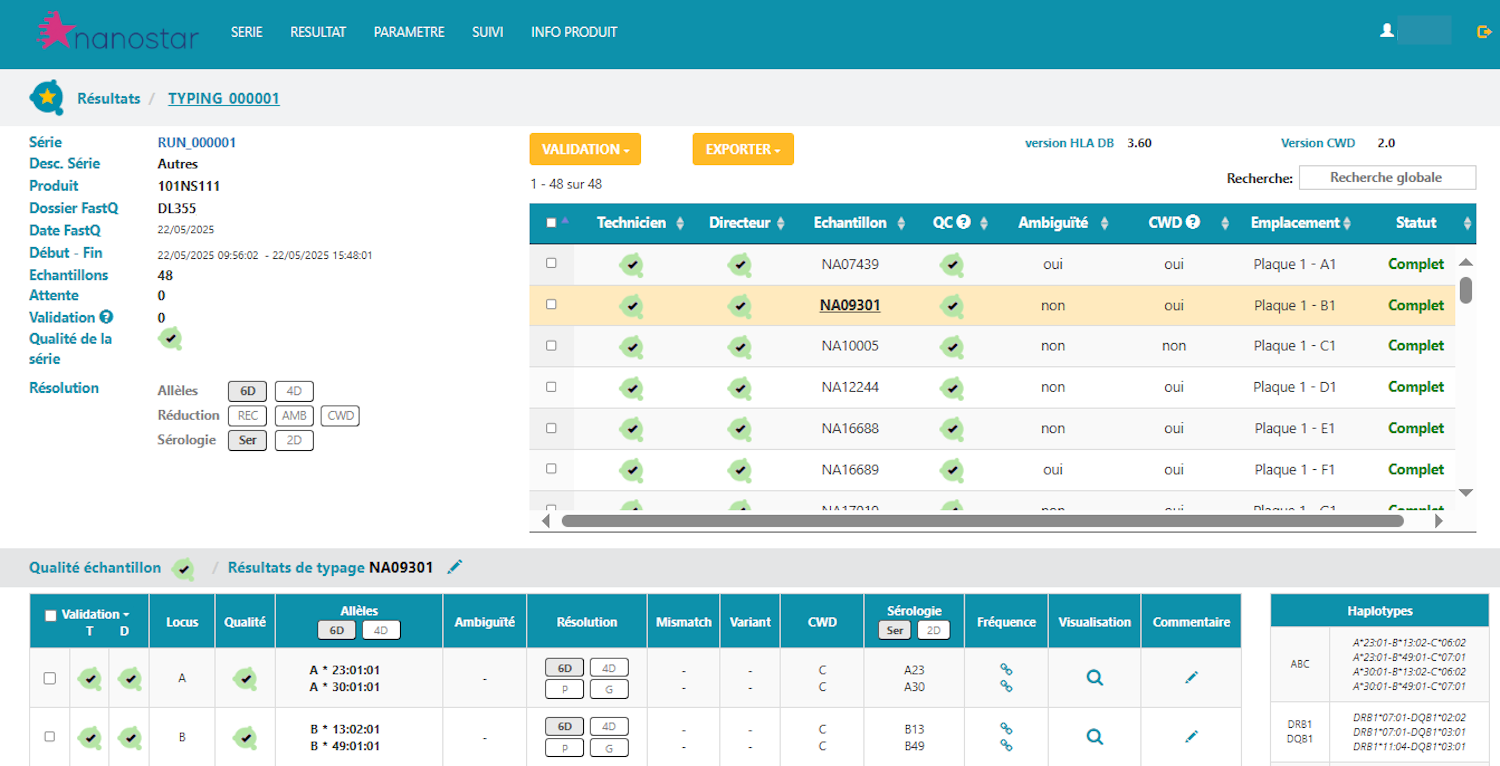
Logiciel d’analyse NanoStar®
Le logiciel NanoStar® NGS HLA Analysis Software est conçu pour interpréter les données de séquençage (FastQ) obtenues grâce aux kits NanoStar®. Il permet d’obtenir des résultats de typage HLA 6 digits pour 48 ou 96 échantillons en moins de 48 heures, avec exportation des résultats compatible LIMs.
Le logiciel intègre :
- Un système de validation automatisée des séries,
- Des contrôles qualité internes (série, échantillons, témoins, loci),
- Une traçabilité complète des fichiers de données brutes, des numéros de série des automates et des lots / dates de péremption des réactifs et consommables utilisés.
- Le logiciel est exclusivement destiné à une utilisation avec les kits NanoStar®, conformément à la notice d’utilisation.
©2025, Bionobis. Tous droits réservés. NanoStar® et Bio-Nano® sont des marques déposées de Bionobis
Bionobis

7 rue Nicolas Copernic, 78280 GUYANCOURT SQY - FRANCE
+33 (0)1 30 43 01 55
info@bionobis.com